-
 28202503國璽專欄
28202503國璽專欄為什麼會得關節炎?可以治好嗎?
生活中過度使用關節、姿勢不良、體重過重或是肌力不足等情況,皆會增加退化性關節炎的罹患率,隨著老化加速疾病惡化,嚴重者甚至造成患者生活品質嚴重下滑。
-
 21202503國璽專欄
21202503國璽專欄INCI Name 是什麼?幹細胞外泌體也能成為化粧品原料?
目前國際已有多家生技公司之幹細胞外泌體通過 INCI Name 審查並取得認證,值得注意的是,然而各家外泌體的製程皆有一定程度的差異性,產品在上市前仍須進行安全性評估。
-
 28202502國璽專欄
28202502國璽專欄從無到有!幫助品牌進軍再生醫學市場
隨著再生醫學的蓬勃發展,幹細胞技術正從醫療領域擴展到生活日常,國璽幹細胞將再生醫療產業鏈垂直整合,開創CDMO/OEM等合作模式,協助合作夥伴加速產品進入市場。
-
 14202502國璽專欄
14202502國璽專欄什麼是生物反應器?幹細胞能大量製造嗎?
生物反應器 (Bioreactor) 為生物製劑在製程放大 (scale-up) 的關鍵設備,製程中須考慮的因素相當複雜,例如細胞特性、環境溫濕度、剪切力、培養基配方等都會影響細胞的生長。
-
 08202501國璽專欄
08202501國璽專欄2024 細胞治療大事蹟
細胞治療的案件數逐年成長,從免疫細胞治療癌症到幹細胞治療退化及組織損傷,細胞治療的廣泛性潛力仍然可期,願再生醫療逐步成為常規醫療的一環。
-
 25202410國璽專欄
25202410國璽專欄外泌體的純化與分析技術:基於MISEV2023的指導準則
《MISEV2023》針對外泌體的研究提出了詳細的純化和分析指導準則,以確保一致性和結果的可靠性。透過多層次的純化技術和精準的分析方法,能更準確地蒐集與鑑別外泌體。
-
 09202410國璽專欄
09202410國璽專欄臨床試驗中的隨機化和盲化試驗
隨機化 (randomization) 和盲化試驗 (blinded) 是臨床試驗中兩個關鍵的方法,用來減少偏差並確保結果的可靠性,是臨床試驗不可或缺的實驗設計方法。
-
 30202409國璽專欄
30202409國璽專欄幹細胞技術:從實驗室到臨床
幹細胞技術已成為再生醫學領域的重要支柱。這項技術不僅在基礎研究中展現出巨大潛力,在臨床應用中備受期待,具潛力成為對多種難治性疾病的治療新選擇。
-
 02202409國璽專欄
02202409國璽專欄細胞治療新藥:從開發到上市
細胞治療新藥從研發到上市的過程通常比傳統小分子藥物更加複雜和嚴格,使細胞治療臨床試驗受到監管單位更嚴格的審查。
-
 30202405國璽專欄
30202405國璽專欄同樣都是先進國家,細胞治療法規差很大?
在全球細胞治療領域,不同國家的法規體系展現出顯著的差異,這些差異影響了研究開發的進度、市場的方向以及患者能獲得的治療選項。
-
 20202405國璽專欄
20202405國璽專欄政府將開放「人類幹細胞來源外泌體」在化妝品中?
衛福部已在2024 年 3月21日訂出了審查標準,預計將於 2024 年 7 月 1 日起實施,「人源外泌體」可經過個案審查通過後正式開放使用。
-
 01202402國璽專欄
01202402國璽專欄「特管辦法細胞治療技術」懶人包
根據衛生福利部統計,從 2018 年 10 月受理特管辦法細胞治療技術申請開始,截至 2023 年 12 月 31 日止,目前已經核准 305 件細胞治療技術施行計畫,總共收案 1,398 人。
-
 24202401國璽專欄
24202401國璽專欄2023 年再生醫療市場有什麼變化?
2023 年再生醫療市場的投資力道雖然因為受通膨影響力道減弱,然而臨床試驗案件跟公司成立數量仍持續增加,顯示儘管投資力道放緩,再生醫學仍是市場重點產業。
-
 18202306國璽專欄
18202306國璽專欄前驅細胞,優化細胞,什麼是條件培養基?
想要從現行的細胞治療產品中脫穎而出,就必須導入特殊製程,例如使用條件培養基 (conditioned medium) 就是一種方法,讓最終產出的細胞製劑可以表達出更好的治療特性。
-
 18202305國璽專欄
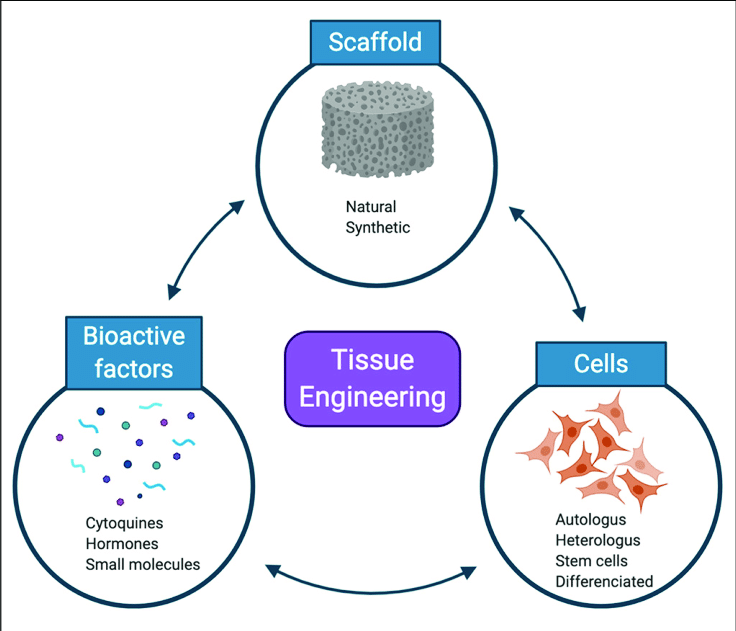
18202305國璽專欄再生醫學中的組織工程是什麼?
在再生醫學的領域中,組織工程是指將細胞治療、生物材料、或合成材料堆疊再一起進行治療,期望在植入後能達到更穩定的狀態。
-
 15202303國璽專欄
15202303國璽專欄什麼是基因導入的細胞治療?
基因導入的細胞治療,是將基因工程技術導入細胞上。若把細胞視為工兵,基因細胞治療就是生化工程兵。但目前基因細胞治療仍有許多需要克服的難題,如細胞失控、細胞風暴等。
-
 14202303國璽專欄
14202303國璽專欄2023國際細胞治療法規動向分享
掌握全球細胞治療趨勢!國璽幹細胞解析各國細胞治療法規動向,協助產業夥伴掌握最新合規策略與市場機會。
-
 12202303國璽專欄
12202303國璽專欄再生雙法對細胞治療產業的影響
為明確定義再生醫療之範疇,加速再生醫療產品之臨床轉譯及醫療品質管理,杜絕不符合品質的細胞治療廠商與不明來源的細胞製劑流通於市面,營造永續發展環境,推動細胞治療產業。
-
 31202007國璽專欄
31202007國璽專欄細胞療法進入商業化生產
商業化生產,首先必須要做到品質的基本要求:均一性和穩定性。細胞治療產品由於原料是活細胞,在本質上就具備有多樣性及不穩定性,在製程管理上挑戰了以往對藥物製造的既有認知。
-
 03201808國璽專欄
03201808國璽專欄幹細胞治療心律不整
國璽幹細胞研發團隊與安南醫院心臟內科部長李聰明醫師合作,由國璽開發適合應用於心血管症狀的幹細胞製劑,提供李聰明醫師以模擬心肌梗塞後產生心律不整的大鼠進行移植治療。

- 國璽除了具備獨特技術平台、專業務實的研發團隊,以及穩定的合作夥伴外,我們積極加強幹細胞技術與整合技術平台,透過多元化的服務與務實策略進行國際化布局,建立細胞治療產業差別化優勢,使國璽成為幹細胞領域的領航者。

- 國璽持續觀察市場變化,在早期已佈局細胞治療產業,致力於開發高市占率的幹細胞新藥,目前已有4支新藥進入臨床試驗階段。除此之外,國璽在生技產業競爭激烈的環境下,發展雙軌併行的營運策略,在開發創新技術的同時提供多樣的技術服務,追求獲利與創新的雙軌成長。

- 國璽幹細胞近年來最大的突破,就是我們開始掌握幹細胞的製藥技術,透過研發專利製程,發揮幹細胞無限應用之潛力。
